本文主要是介绍单细胞专题 | 带你“走近”单细胞转录组测序,希望对大家解决编程问题提供一定的参考价值,需要的开发者们随着小编来一起学习吧!
◆ 单细胞测序的概念 ◆
上节我们讲到转录组测序相关内容,这期将继续学习单细胞转录组测序。单细胞测序技术(single cell sequencing),简单来说,就是在单个细胞水平上,对基因组、转录组及表观基因组进行测序分析的技术(图1)。

图1.单细胞测序技术
◆ 为什么做单细胞转录组测序? ◆
普通转录组(bulk RNA-seq)是生物组织样品中在某个时间对应的所有mRNA转录情况,可以作为组织或者样品某个时刻状态的重要指标。然而,不同物种、组织以及处理都会造成mRNA表达情况的改变,从而调控机体的生命活动和改变细胞功能。与蛋白质相比较,mRNA的稳定性和易检测性大大促进了转录组技术的应用和发展。但是普通转录组测序测到的结果是所有细胞的一个转录组表达量的平均值,它不能反映样品中所有细胞或者某群细胞特有的状态。
因此科学家发明了单细胞转录组测序,以此对单个细胞的或者某群细胞的转录状态进行深入的研究,这样会更精细、更准确的反映组织的状态。特别是在医学的研究中,可以更精准地针对细胞或者细胞亚群进行免疫治疗或者靶向治疗,从而在生物体的功能机制的解析和发现更为有效的疾病治疗方法等方面具有更广阔的应用前景。
◆ 单细胞捕获技术的发展 ◆
单细胞类实验的最重要的一步就是单个细胞的捕获,早期的单细胞获取方式,是通过一定的技术手段,将单个细胞分离出来,并利用SMART-Seq2或商业化的SMART-Seq4试剂独立构建测序文库,最终进行测序。捕获方式包括:有限稀释法、流式分选法、激光切割法、显微操作法(图2前四种)。这些方法虽然各有各的优点,但各自的缺点也十分明显,比如流式分选法对于浓度的计算易存在误差;流式分选法不适用于微量样本;激光切割法操作复杂;显微切割法的细胞通量低等。而它们的共同缺点,就是捕获成本高。

图2. 单个细胞的主要分选方式
随着单细胞测序技术的发展,越来越多快速低成本的单细胞捕获技术被发明出来。目前应用最多的是微流控技术(图2最后一种)。以目前占全球95%市场份额的10X Genomics Chromium转录组测序为例,它主要是将细胞与逆转录试剂预混在一起,通过微流控芯片的一条通道,与另一通道中的携带百万个不同barcode(标签)的gel beads(凝胶珠)相遇,穿过油幕的同时被包裹在一个油滴中,便可以轻松得到一个细胞和一个凝胶珠包在一起的油包水滴GEMs(图3)。其核心技术是将不同的细胞赋予一段不同的barcode序列,建库时,携带相同barcode序列的核酸分子被认为来自同一个细胞,这样我们就可以从成千上万个细胞中顺利区分它们。这些技术的出现,让快速、低成本地分析数千个单细胞的基因活性成为现实。

图3.单细胞分选与标记
◆ 单细胞转录组测序流程 ◆
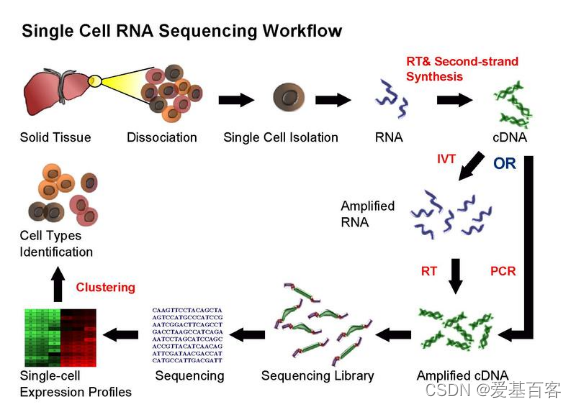
图4.单细胞RNA-seq实验流程
前面已经介绍了单细胞的捕获与分选,接下来我们看一下转录组测序的实验流程,大致分为以下几个步骤,动植物组织样本的准备、组织样本酶解成单个细胞细胞悬液制备与质检、barcode标记细胞、mRNA反转录、文库的构建、高通量测序和数据分析。为了保证实验结果的可靠性、重复性和准确性,在第一步动植物样本的准备阶段,一般需要遵从以下原则:
(1) 样品总量:一个样本的细胞起始量需>1 x 105个;
(2)样品浓度:最终上样前细胞浓度在700-1200 cells /μL ;
(3)细胞活性:活细胞数目>85%;
(4)细胞大小:直径<40μm ;
(5)细胞培养基及缓冲液不能含有 Ca +和 Mg 2+等影响酶活性的物质:
(6)组织需解离成单细胞悬液,这里需要特别注意的是单细胞植物样本的制备较为复杂,大致分为两种手段,原生质体的制备和提核。
小Tips:如果无法满足单细胞制备要求,也可以考虑单细胞核制备,也更适合于冻存样本。
具体的送样方法和细节可以联系我们的销售人员。
◆ 单细胞转录组测序的应用 ◆
1) 医学方向的应用案例
骨髓纤维化的特征是骨髓中的造血细胞被过多的瘢痕组织持续替换。原发性骨髓纤维化(PMF)是骨髓纤维化进行性发展的典型例子。显性PMF的显著特征是细胞外基质(ECM)的过度沉积,伴随的是骨髓外造血导致的渐进性造血丧失和脾肿大。虽然造血细胞中驱动骨髓增生性肿瘤(MPN)发展的分子改变已基本确定,但骨髓增生性肿瘤患者骨髓微环境中单个细胞成分对骨髓纤维化(MF)的功能作用尚不完全清楚。

2020年12月,来自荷兰的Erasmus医学中心Rebekka K. Schneider团队在Cell Stem Cell上发表题为 “Heterogeneous bone-marrow stromal progenitors drive myelofibrosis via a druggable alarmin axis” 的文章。作者通过单细胞转录组分析小鼠和人骨髓纤维化中骨髓基质细胞组成,确定了纤维化驱动细胞和潜在机制。

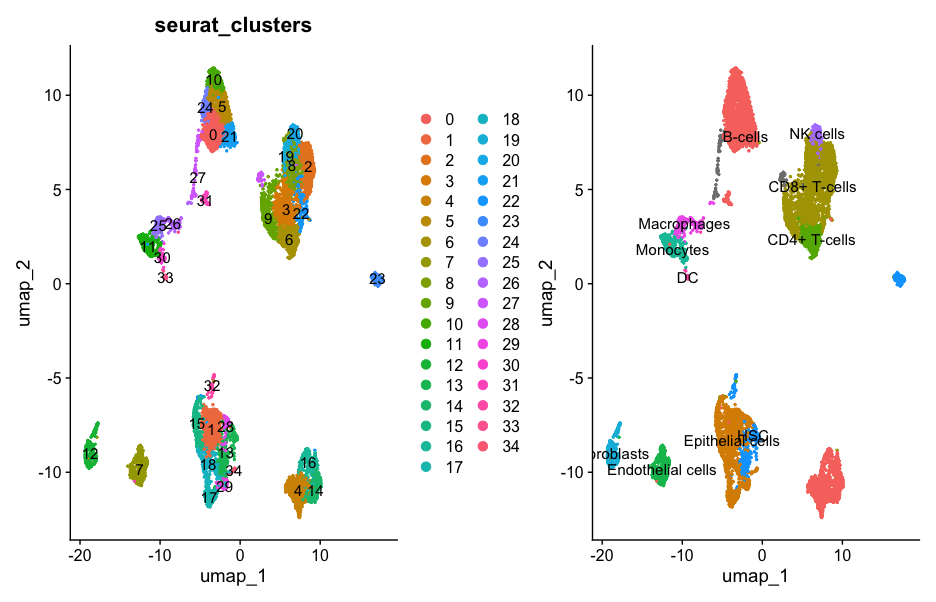
图5. 8个不同的非造血细胞群的鉴定
在本研究中[1],作者通过单细胞RNA测序对纯化的非造血骨髓细胞进行特异性分析,以确定MPNs中的纤维化驱动细胞和潜在机制,从而探索小鼠和人类BM基质的细胞组成。研究结果确定两种不同的间充质干细胞群体(MSC-1和MSC-2)是骨髓间充质干细胞纤维化的主要驱动因素。研究结果还显示两个不同的间充质基质细胞(MSC)亚群为促纤维化细胞。MSC以阶段依赖的方式进行功能重组,在纤维化前开始分化,在纤维化阶段获得促纤维化和炎症表型。此外,MSC中蛋白复合物S100A8/S100A9的表达标志着疾病在小鼠模型、患者基质和血浆中向纤维化阶段进展。而Tasquinimod是一种抑制S100A8/S100A9信号传导的小分子,可显著改善JAK2V617F突变小鼠模型的MPN表型和纤维化,这说明S100A8/S100A9是MPN治疗中非常有吸引力的一个治疗靶点,可以为今后骨髓瘤的治疗提供参考方向。
2) 植物方向的应用案例
植物是由各种类型的细胞组成的,它们作为一个整体发挥作用,以确保成功的营养生长。由于这些细胞携带着几乎相同的遗传信息,功能上的变化是由细胞分化过程中转录活动的程序化调节产生的。因此,了解单细胞转录组的异质性将为植物生理和发育提供独特的见解。

2021年6月,中国科学院遗传与发育生物学研究所钱文峰研究员团队在《Journal of Genetics and Genomics》杂志在线发表了题为“Single-cell transcriptome atlas of the leaf and root of rice seedlings”的研究论文,该研究以水稻幼苗叶片和根系为研究对象,通过转录组测序构建了其单细胞转录组图谱。

图6. 水稻根系单细胞转录组图谱
在本研究中[2],作者利用单细胞RNA测序技术绘制水稻幼苗叶片和根系的单细胞转录图谱。作者首先对生长在Kimura B营养液或暴露于各种非生物胁迫下的水稻幼苗的茎和根进行了单细胞RNA测序,并对总共237431个单个细胞的转录组进行了表征。作者分别在叶和根中识别出15和9种细胞类型,并观察到同一组织层的叶和根之间通常共享共同的转录组特征。非生物应激刺激很大程度上以细胞类型特有的方式改变基因表达,但对于给定的细胞类型,不同的应激通常会引发大致相同的一组基因的转录调控。此外,作者还检测了细胞群在响应非生物胁迫时的比例变化,并通过单细胞重建发育轨迹来研究潜在的分子机制。总之,该研究结果显示了单细胞RNA测序在水稻上的应用能力,并为植物细胞图谱的构建铺平了道路。
◆ 总 结 ◆
总之,单细胞转录组测序不仅可以揭示每个细胞独特的变化,而且还可以发现全新的细胞类型,极大地推动了基因组学研究。目前,单细胞转录组技术在人类和小鼠等动物中研究较多,包括细胞群的分类研究、细胞表达谱的检测以及区分细胞类型组成或细胞状态的差异:如肿瘤细胞异质性、病理诊断、细胞周期等。此外,单细胞转录组测序也可以应用于植物方向,如在拟南芥、水稻、番茄和玉米中都有研究。
在单细胞测序方面,爱基百客先后引进10x Genomics 单细胞平台、寻因单细胞平台,为客户提供单细胞转录组、单细胞ATAC、空间转录组等科研服务,可以提供从前期样本制备到后期数据分析的完整服务,已协助客户在Protein & Cell、 Journal of Hematology & Oncology等杂志发表诸多高水平文章。有相关需求的老师可以联系我们哦!
参考文献:
[1] Leimkuehler N B , Gleitz H , Li R , et al. Heterogeneous bone-marrow stromal progenitors drive myelofibrosis via a druggable alarmin axis[J]. Cell Stem Cell, 2020.
[2] Yu W , Qh A , Ke L A , et al. Single-cell transcriptome atlas of the leaf and root of rice seedlings[J]. Journal of Genetics and Genomics, 2021.
这篇关于单细胞专题 | 带你“走近”单细胞转录组测序的文章就介绍到这儿,希望我们推荐的文章对编程师们有所帮助!