本文主要是介绍Lancet| 好的RCT文章不在于统计,在设计!K-M分析+COX比例风险模型即可,希望对大家解决编程问题提供一定的参考价值,需要的开发者们随着小编来一起学习吧!
郑老师统计课程,欢迎点击报名:孟德尔随机化课程即将开班!!
2023年9月,外国学者在《Lancet》(一区,IF=168.9)发表题为:" Adjuvant immunotherapy with nivolumab versus observation in completely resected Merkel cell carcinoma (ADMEC-O): disease-free survival results from a randomised, open-label, phase 2 trial" 的研究论文。
在德国和荷兰的20个学术医疗中心,完全切除默克尔细胞癌病变的患者以2∶1的比例被随机分配接受纳武利尤单抗或观察。我们的目的是评估佐剂免疫检查点抑制在完全切除的MCC(即没有建立系统标准治疗的环境)中的有效性和安全性。结果表明,纳武单抗辅助治疗导致绝对风险降低9%(1年DFS)和10%(2年DFS)。

摘要与主要结果
一、摘要
背景:默克尔细胞癌(MCC)是一种免疫原性的侵袭性皮肤癌。即使在完全切除和放疗后,复发率也很高。PD-1和PD-L1检查点抑制剂在晚期MCC中显示出临床益处。我们的目的是评估佐剂免疫检查点抑制在完全切除的MCC(即没有建立系统标准治疗的环境)中的有效性和安全性。
方法:在这项多中心2期试验中,在德国和荷兰的20个学术医疗中心,完全切除MCC病变的患者(任何分期,美国东部肿瘤协作组体能状态评分0 ~ 1分)以2∶1的比例被随机分配接受纳武利尤单抗480 mg治疗,每4周1次,持续1年,或观察,并根据分期(美国癌症联合委员会1 ~ 2期vs 3 ~ 4期)、年龄(<65岁vs≥65岁)和性别进行分层。12个月和24个月的标志性无病生存期(DFS)是主要终点,在意向治疗人群中进行评估。总生存期和安全性是次要终点。当最后一位患者随访超过1年时,启动了计划中的中期分析。本研究已在ClinicalTrials.gov(NCT02196961)和欧盟临床试验注册系统(european ClinicalTrials Register, 2013-000043-78)注册。
结果:2014年10月1日至2020年8月31日,纳入179例患者(116例[65%],3-4期,122例[68%],≥65岁,111例[62%]男性)。分层因素(分期、年龄、性别)在纳武单抗组(n=118)和内部对照组(n= 61)之间得到平衡;辅助放疗在对照组中更为常见。中位随访24.3个月(IQR 19.2 - 33.4),中位DFS未达到(组间风险比0.58,95% CI 0.30 - 1.12);纳武单抗组12个月时的DFS率为85%,24个月时为84%,观察组12个月时为77%,24个月时为73%。总体生存结果尚不成熟。115例至少接受一次纳武单抗治疗的患者中有48例(42%)发生了3-4级不良事件,观察组61例患者中有7例(11%)发生了不良事件。没有与治疗相关的死亡报告。
结论:纳武单抗辅助治疗导致绝对风险降低9%(1年DFS)和10%(2年DFS)。目前ADMEC-O的中期分析可能建议在这一未满足医疗需求的领域临床使用纳武单抗。然而,总的生存事件发生率,积极治疗组有10个事件,一半大小观察组有6个事件,还不够成熟,无法得出结论。我们试验的探索性数据支持该领域正在进行的随机试验的继续。ADMEC-O提示辅助免疫治疗在这一未满足医疗需求的领域是临床可行的。
二、研究结果
1.患者
从2014年10月1日到2020年8月31日,来自德国19个学术中心和荷兰1个中心的179名患者被纳入并随机分配(表1)。在随机分配到尼武单抗组的118名患者中,只有115名患者接受了至少一剂指定治疗,因为3名患者在随机分配后不久撤回了知情同意。每12周安排一次疾病评估的随访,两组的随访时间相似(纳武单抗组平均3.2个月,观察组平均3.4个月;差异-0.2,95% CI-0.4至0.0)。而观察组术后接受辅助放疗的患者比例更高(45例[74%]vs 59例[50%])。每组1例患者伴有相关的免疫损害血液病。
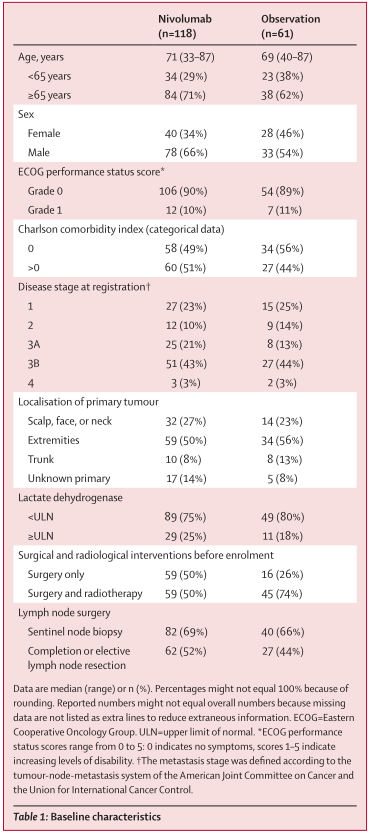
2.基线特征
在这项中期分析的截止日期(2022年4月5日),所有接受纳武单抗治疗的患者均已结束治疗;其中67例完成了12个月的治疗(图1)。在纳武单抗组中48例未完成完整疗程的患者中,主要原因是治疗相关毒性(n=17)和复发事件(n=12)。纳武单抗组86例患者和观察组48例患者仍在随访中(图1)。该中期分析的总中位随访时间为24.3个月(IQR为19.2-33.4):纳武单抗组26.3个月(19.7-34.8),观察组23.4个月(18.2-27.9)。积极治疗组的中位剂量数为12 (IQR 7-13),治疗的中位时间为48.0周(IQR 25.1-48.1)。
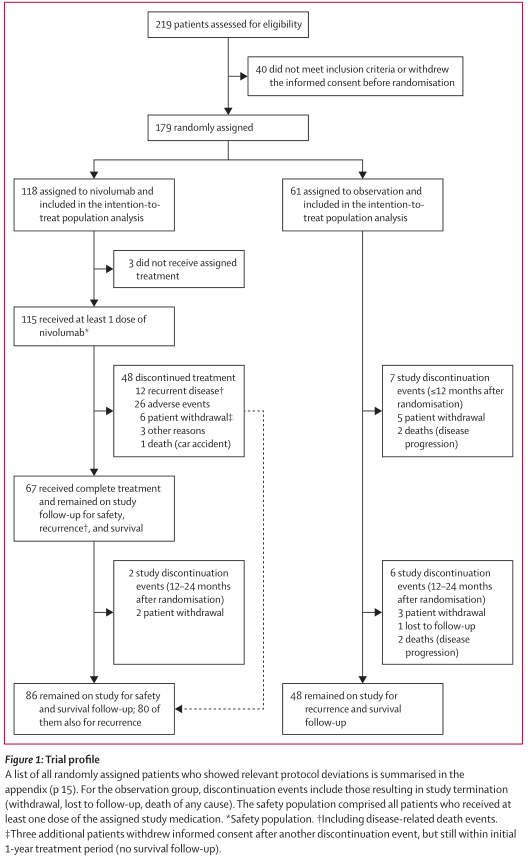
3.主要结果
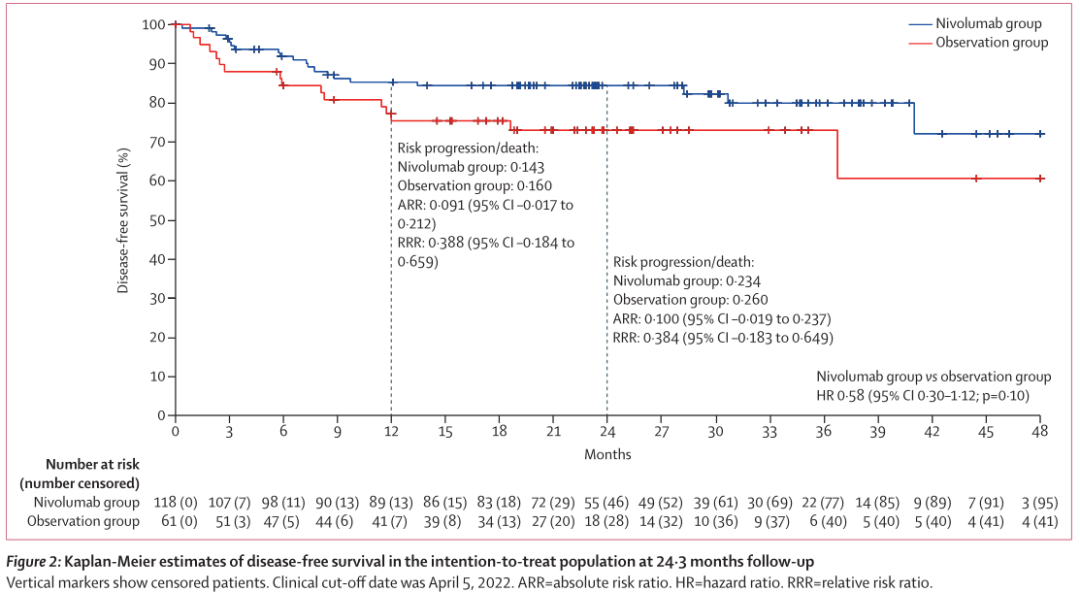
截至数据截止,纳武单抗组有20例疾病复发或死亡事件,1年DFS为85% (95% CI 77-91), 2年DFS为84% (76-90);中位生存期(DFS)尚未达到(图2)。1年和2年总生存率评分相等,为94% (95% CI 87-97), 10例死亡后,中位总生存率未达到。观察组共发生16例;1年DFS为77% (95% CI 64-86), 2年DFS为73%(59-83)。有6例死亡记录,1年生存率为96%(87-99),2年生存率为92%(80-97)。根据预先指定的分层因素(疾病阶段、性别和年龄)对两个治疗组的1年和2年DFS率进行分层。
与观察组相比,12个月和24个月时DFS的Kaplan-Meier估计值之间的风险差异显示,积极治疗组1年的绝对风险降低0.091(95% CI -0.02至0.21),2年的绝对风险降低0.10(-0.02至0.24)(图2)。12个月时相应的相对风险降低为0.388 (95% CI -0.184至0.659),24个月时相应的相对风险降低为0.384 (95% CI -0.183至0.649)。由于观察组的复发风险远低于历史数据,即使本试验中几乎三分之二的患者患有3期或更高的疾病,相对风险差异与评估辅助治疗的潜在益处相关。
通过方案特定变量对DFS进行的Cox回归分析一致表明,治疗组之间的差异优于观察组;然而,风险比95%CI均超过阈值线,因为在中期分析中仍观察到低事件发生率(图3)。由于大多数患者在基线时处于3期,因此对3A和3B期患者进行了探索性分析,以进一步阐明这两个预后阶段的临床病程。
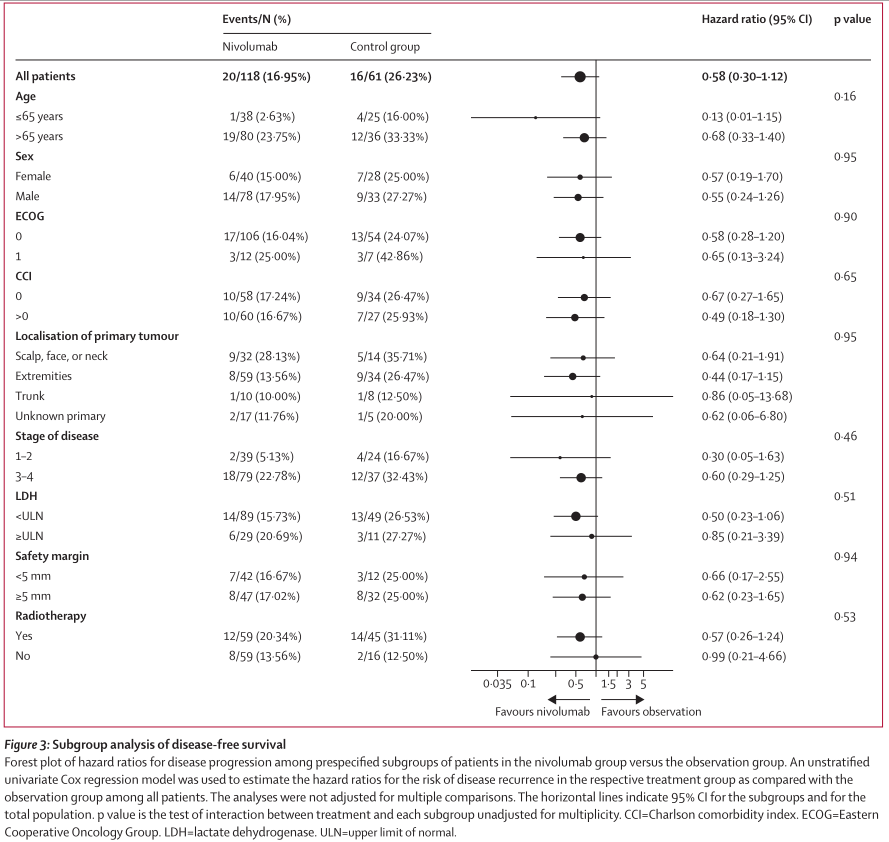
局部复发或复发是纳武单抗组(15例复发中有9例[60%])和观察组(13例复发中有10例[77%])复发的主要模式;探索性疗效终点、转化生物标志物分析和生活质量数据将在稍后报告(最终分析)。
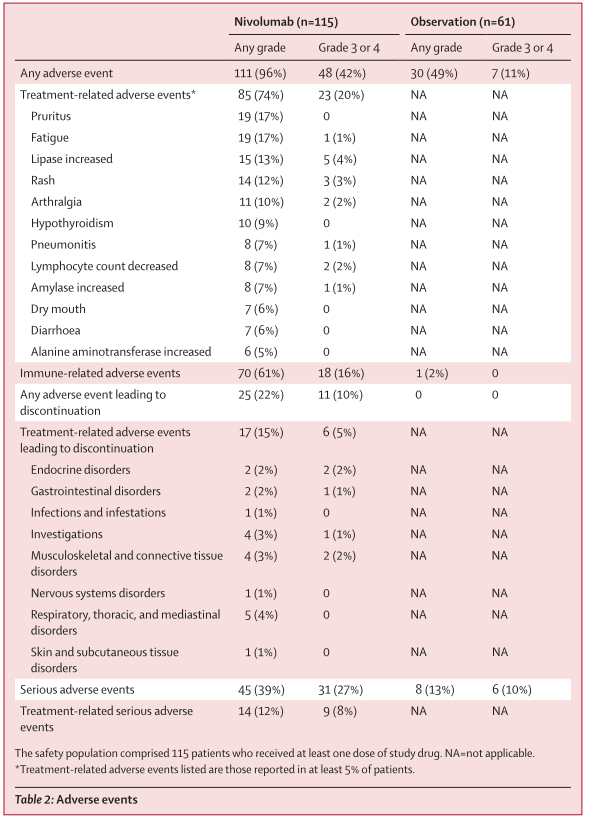
4.不良结果
在接受至少一剂纳武单抗的115例患者中,有111例(97%)发生任何原因的不良事件;在观察组中,61例患者中有30例(49%)记录了不良事件(表2)。两组中3级或4级不良事件发生频率的差异为31%(95% CI 19-43),纳武单抗组115例患者中有48例(42%),观察组61例患者中有7例(11%)。85例(74%)患者发生任何级别的治疗相关不良事件,23例(20%)患者发生3-4级不良事件。瘙痒、疲劳和任何级别的脂肪酶升高是仅有的总频率超过10%的治疗相关事件。脂肪酶浓度高于正常上限两倍是唯一发生在2例以上患者中的3-4级事件(表2)。
纳武单抗组115例患者中有70例(61%)发生任何级别的免疫相关不良事件;18例(16%)患者发生3-4级免疫相关事件。免疫介导性垂体炎发生两次,是唯一出现在1名以上患者中的3-4级事件;单一事件包括胰腺炎、肝炎、肌炎和1型糖尿病各1例。
25例(22%)患者发生任何级别的不良事件导致停止治疗;在17例(15%)病例中,不良事件被归类为治疗相关,其中只有6例(5%)为3-4级(表2)。与治疗相关的不良事件发生和消退的中位时间见附录。
没有与治疗相关的死亡报告。在最初的12个月治疗或观察期间,有5名患者死亡;纳武利尤单抗组3例患者(2例在既往疾病复发并随后停止治疗后发生疾病进展,1例发生与治疗无关的交通事故)和观察组2例患者(疾病进展)。
设计与统计学方法
一、研究设计
P(Population)参与者:2014年10月1日至2020年8月31日来自德国和荷兰20个学术医疗中心的完全切除MCC病变的患者。
E(exposure)暴露因素:接受纳武利尤单抗480 mg治疗,每4周1次,持续1年,或观察。
O(outcome)结局:12个月和24个月的标志性无病生存期(DFS)是主要终点。
S(Study design)研究类型:多中心、随机、开放标签、2期试验的临床试验。
二、统计方法
1.这项随机、开放标签的2期试验的主要目的是评估辅助纳武单抗单药治疗完全切除的MCC患者的疗效。为了评估积极治疗的疗效,主要研究变量DFS被评估为纳武利尤单抗和观察之间的风险差异,使用12个月和24个月的Kaplan-Meier估计值进行比较。对于这个具有里程碑意义的分析,使用了描述性统计。根据Cox比例风险模型估计绝对和相对风险降低;采用bootstrap估计绝对风险降低和相对风险降低的CI。


2.样本量计算
假设最初的累积时间为36个月,随访时间为24个月,退出率为10%,计算出177例患者的样本量,结果(2:1分布)积极治疗组118例,仅观察组59例。由于观察到的事件数量低于原始样本量计算中预期的数量,因此将里程碑分析假设调整为使用90% CI评估统计不确定性的描述性统计。然而,尽管统计分析计划要求使用导出的90%线性CI作为常见的点向CI来评估统计不确定性为了便于与其他研究进行比较,我们在这里报告了更严格的标准95% CI。使用临床研究的样本量表进行样本量计算。

3.统计分析提供了参与者数量、缺失观测值、平均值、中位数(95% CI)标准差、四分位数范围、最小值和最大值。所有疗效分析均基于两组所有随机患者组成的完整分析集;安全性分析包括接受至少一剂纳武单抗的积极治疗组的所有随机患者。随着2021年4月签署的最后一项协议修正案,统计分析计划中增加了一项中期分析,以评估和临时评估试验的收益-风险。一旦最后一位患者随访至少1年,就安排中期分析。

一个专门做公共数据库的公众号,关注我们

这篇关于Lancet| 好的RCT文章不在于统计,在设计!K-M分析+COX比例风险模型即可的文章就介绍到这儿,希望我们推荐的文章对编程师们有所帮助!







