本文主要是介绍PD-L1表达与免疫逃逸和免疫响应,希望对大家解决编程问题提供一定的参考价值,需要的开发者们随着小编来一起学习吧!
免疫检查点信号转导和癌症免疫治疗(文献)-CSDN博客 https://blog.csdn.net/hx2024/article/details/137470621?ops_request_misc=%257B%2522request%255Fid%2522%253A%2522171551954416800184136566%2522%252C%2522scm%2522%253A%252220140713.130102334.pc%255Fblog.%2522%257D&request_id=171551954416800184136566&biz_id=0&utm_medium=distribute.pc_search_result.none-task-blog-2~blog~first_rank_ecpm_v1~rank_v31_ecpm-2-137470621-null-null.nonecase&utm_term=PD-L1&spm=1018.2226.3001.4450
https://blog.csdn.net/hx2024/article/details/137470621?ops_request_misc=%257B%2522request%255Fid%2522%253A%2522171551954416800184136566%2522%252C%2522scm%2522%253A%252220140713.130102334.pc%255Fblog.%2522%257D&request_id=171551954416800184136566&biz_id=0&utm_medium=distribute.pc_search_result.none-task-blog-2~blog~first_rank_ecpm_v1~rank_v31_ecpm-2-137470621-null-null.nonecase&utm_term=PD-L1&spm=1018.2226.3001.4450
目录
①PD-1、PD-L1与抗PD-1治疗的关联
基本介绍
讨论
②PD-L1作为对免疫检查点抑制剂反应的生物标志物
③肺癌中Nivolumab与PD-L1表达水平
肺癌nivolumab研究
PD-L1表达水平与疗效无关
①PD-1、PD-L1与抗PD-1治疗的关联
Association of PD-1, PD-1 ligands, and other features of the tumor immune microenvironment with response to anti-PD-1 therapy - PubMed (nih.gov)
基本介绍
实验设计:黑色素瘤、非小细胞肺癌(NSCLC)、肾细胞癌(RCC)、结直肠癌或抗阉割前列腺癌患者(N = 41)在一家机构接受了抗PD-1(nivolumab)的早期试验治疗,并有可评估的治疗前肿瘤标本。研究人员评估了免疫结构特征,包括PD-1、PD-L1和PD-L2的表达、免疫细胞浸润模式和淋巴细胞亚群,以确定它们与临床结果之间的相互关系和潜在关联。
结果:不同肿瘤类型的肿瘤细胞和免疫浸润细胞的膜性(细胞表面)PD-L1表达量差异很大,黑色素瘤、NSCLC和RCC的表达量最高。在总体队列中,PD-L1的表达与浸润免疫细胞的地理分布相关(P<0.001),尽管淋巴细胞丰富的区域并不总是与PD-L1的表达相关。肿瘤细胞和免疫浸润细胞的PD-L1表达与淋巴细胞上的PD-1表达明显相关。PD-1的第二配体PD-L2与PD-L1的表达有关。在分析最接近治疗的标本或患者多个活检样本中得分最高的样本时,肿瘤细胞 PD-L1 表达与抗 PD-1 治疗的客观反应相关。这些相关性强于PD-1表达或瘤内免疫细胞浸润与反应的边缘相关性。
讨论
观察表明,这也可能适用于 PD-1 通路阻断。在目前的研究中,肿瘤表达PD-L1的患者更有可能对抗PD-1治疗有反应。尽管 PD-L1 通常被视为一种免疫抑制分子,但其表达并不一定等同于肿瘤免疫逃避,并且可能反映了持续的抗肿瘤免疫应答,包括 IFNγ 和其他炎症因子的产生。
尽管 PD-L1+ 患者群体的反应率有所提高,但目前尚不清楚为什么大多数 PD-L1+ 患者对 PD-1 通路阻断药物没有反应。一种可能性是,来自无反应者的 PD-L1+ 肿瘤表达了额外的显性或共显性免疫检查点,支持治疗耐药性。为了解决这个问题,我们检查了PD-L2(PD-1的第二个已知配体)与PD-L1表达和临床结果的可能关联。IHC 检测到的 PD-L2 蛋白几乎完全与 PD-L1 蛋白在位置上相关,这与其已知的炎症细胞因子上调一致,包括 IFNγ,IFNγ 也驱动 PD-L1 表达 。然而,在我们的系列研究中,PD-L2 表达的频率低于 PD-L1(在检查的 38 个标本中仅存在 8 个),并且未观察到与临床结果的显着相关性。尽管我们的系列研究结果应被视为初步结果,但最近一份关于在接受抗 PD-L1 治疗的患者中通过定量分子技术检测到 PD-L2 表达的报告得出了类似的结论 。我们的实验室目前正在进行旨在确定对抗 PD-1 治疗反应的其他阳性或阴性预测标志物以及肿瘤微环境中多种因素之间潜在相互作用的研究。
②PD-L1作为对免疫检查点抑制剂反应的生物标志物
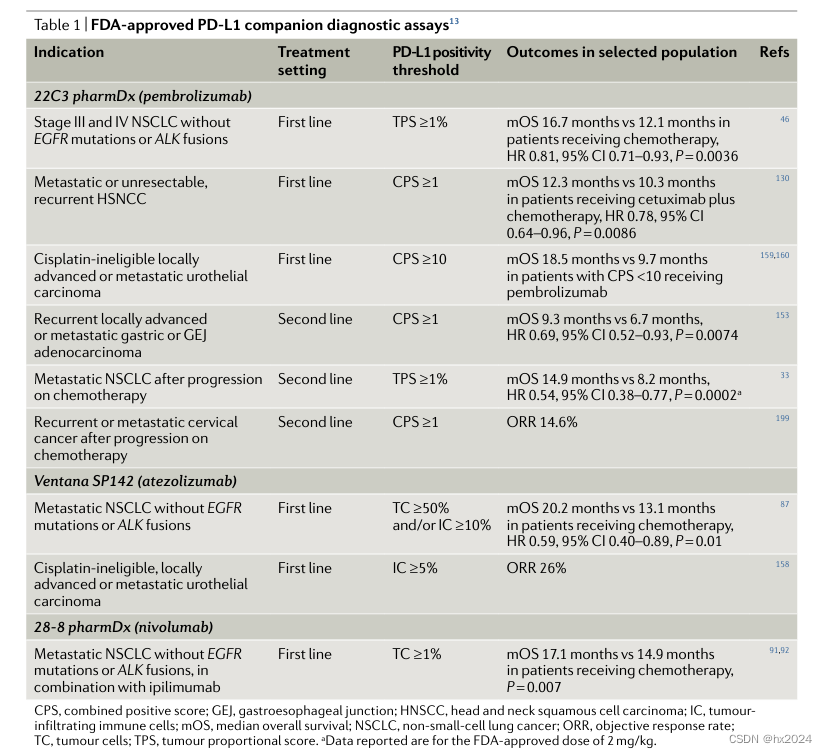
PD-L1 as a biomarker of response to immune-checkpoint inhibitors - PubMed (nih.gov)
主要介绍了PD-L1的检测手段
③肺癌中Nivolumab与PD-L1表达水平
Nivolumab versus Docetaxel in Advanced Squamous-Cell Non–Small-Cell Lung Cancer - PMC (nih.gov)
肺癌nivolumab研究
方法:我们随机分配了272名患者接受尼妥珠单抗(每公斤体重3毫克,每两周一次)或多西他赛(每平方米体表面积75毫克,每三周一次)治疗。主要终点是总生存期。
结果:nivolumab的中位总生存期为9.2个月(95%置信区间[CI],7.3-13.3),而多西他赛的中位总生存期为6.0个月(95%置信区间[CI],5.1-7.3)。nivolumab的死亡风险比多西他赛低41%(危险比为0.59;95% CI为0.44至0.79;P<0.001)。1年后,nivolumab的总生存率为42%(95% CI,34至50),而多西他赛为24%(95% CI,17至31)。nivolumab的应答率为20%,多西他赛为9%(P=0.008)。nivolumab的中位无进展生存期为3.5个月,而多西他赛为2.8个月(死亡或疾病进展危险比为0.62;95% CI为0.47至0.81;P<0.001)。PD-1配体(PD-L1)的表达既不是预后指标,也不是获益的预测指标。7%的nivolumab组患者报告了3级或4级治疗相关不良事件,而55%的多西他赛组患者报告了3级或4级不良事件。
结论:在既往接受过治疗的晚期鳞状细胞NSCLC患者中,无论PD-L1表达水平如何,尼妥珠单抗的总生存期、应答率和无进展生存期都明显优于多西他赛。(由百时美施贵宝资助;CheckMate 017 ClinicalTrials.gov编号:NCT01642004)。
PD-L1表达水平与疗效无关
在这项研究中,无论肿瘤PD-L1表达水平如何,都观察到了nivolumab的疗效,包括生存获益,结果表明PD-L1表达既不是鳞状细胞NSCLC患者的预后指标,也不是疗效的预测指标。这些分析的局限性在于,PD-L1表达是在存档肿瘤组织中评估的,可能无法反映治疗时的肿瘤PD-L1状态,而且只有83%接受随机化的患者有可量化的PD-L1表达。我们认为,PD-L1表达与疗效之间缺乏关联可能与PD-L1检测的性能无关,而是肿瘤与免疫系统之间复杂相互作用的结果。
总之,纳武利尤单抗是一种PD-1检查点抑制剂,在既往接受过治疗的晚期鳞状细胞NSCLC患者中,与目前的标准治疗相比,显示出具有临床意义的生存获益,安全性有所提高。无论研究前 PD-L1 表达水平如何,都观察到益处。需要进一步的研究来确定具有足够敏感性和特异性的相关生物标志物,以预测哪些患者最有可能受益。
参考文献:
1,Association of PD-1, PD-1 ligands, and other features of the tumor immune microenvironment with response to anti-PD-1 therapy
2,PD-L1 as a biomarker of response to immune-checkpoint inhibitors
3,Nivolumab versus Docetaxel in Advanced Squamous-Cell Non–Small-Cell Lung Cancer
这篇关于PD-L1表达与免疫逃逸和免疫响应的文章就介绍到这儿,希望我们推荐的文章对编程师们有所帮助!






